Veja quais são as vacinas contra a Covid-19 que estão em teste em humanos ao redor do mundo
Publicado em: 21 de outubro de 2020 | Atualizado: outubro 21, 2020
Pesquisadores de todo o mundo buscam por uma candidata segura e eficaz para vacina contra o novo coronavírus. Até a última atualização desta reportagem, em 21 de outubro, a Organização Mundial da Saúde (OMS) já havia registrado cerca de 179 pesquisas em desenvolvimento, com ao menos 44 delas sendo testadas em humanos – destas, 10 estão na terceira e última fase.
A China é o país com mais candidatas em Fase 3 na corrida por uma imunização, com quatro vacinas experimentais (leia mais sobre as etapas adiante); Estados Unidos, Alemanha, Reino Unido e Rússia também têm pesquisas avançadas. Veja quais são as 10 vacinas nesta etapa:
Vacinas em Fase 3 dos testes em humanos
| Laboratório | Nome da vacina | Tipo de imunização | País |
| Janssen Pharmaceutical Companies | Ad26 SARS-CoV-2 | Vetor Viral | EUA |
| Moderna/Instituto Nacional de Alergia e Doenças Infecciosas | mRNA 1273 | Genética | EUA |
| BioNTech/Fosun Pharma/Pfizer | BNT162 | Genética | EUA, Alemanha |
| Universidade de Oxford/AstraZeneca | AZD1222 | Vetor Viral | Reino Unido |
| Sinovac | CoronaVac | Inativado | China |
| Instituto de Produtos Biológicos de Wuhan/Sinopharm | ? | Inativado | China |
| Instituto de Produtos Biológicos de Pequim/Sinopharm | ? | Inativado | China |
| CanSino Biological Inc./Instituto de Biotecnologia de Pequim | AD5-nCov | Vetor Viral | China |
| Novavax | NVX-CoV2373 | Subunidade de proteína | EUA |
| Instituto de Pesquisa Gamaleya | Sputinik V | Vetor Viral | Rússia |
Sputnik V (Rússia)
A vacina russa Sputnik V, desenvolvida pelo Instituto Gamaleya está, segundo a OMS, na terceira fase de testes em humanos. O estudo mais recente publicado na revista científica “The Lancet” em 4 de setembro indicou que a candidata russa não teve efeitos adversos e induziu resposta imune.
Os cientistas reconheceram, no entanto, a necessidade de mais testes para comprovar a eficácia da vacina. Ainda assim, o governo da Rússia já autorizou a produção deste imunizante em grande escala, medida que foi criticada pela comunidade internacional.
Rússia registra 1ª vacina contra a Covid-19: 5 pontos para entender
AZD1222 (Reino Unido)
Mais conhecida no Brasil como a vacina da Universidade de Oxford, a AZD1222 é a que está há mais tempo na Fase 3 dos testes em humanos. Ela usa um adenovírus que afeta chimpanzés para transportar o RNA do Sars-Cov-2 para dentro do corpo humano.
Ela começou seus testes em milhares de voluntários ainda em abril e foi a primeira a ser testada no Brasil, com 5 mil voluntários em 3 estados. Segundo o Ministério da Saúde, caso seja aprovada na terceira fase, 30 milhões de doses dessa vacina serão distribuídas no Brasil em janeiro de 2021.
Cientistas de Oxford relatam vacina segura e com resposta imune
mRNA1273 (EUA)
A candidata da farmacêutica norte-americana Moderna, desenvolvida com apoio do governo dos Estados Unidos, é feita a partir do RNA mensageiro – por isso o nome mRNA – que introduz no corpo humano um pedaço do código genético da proteína S do vírus, ensinando-o como responder a uma futura infecção.
A vacina recebeu uma autorização especial da agência de vigilância sanitária dos EUA (FDA da sigla em inglês) que autorizou a equipe de pesquisadores a avançar, de maneira mais rápida, para as fases finais do estudo.
Laboratório americano começa testes da vacina contra a Covid-19 em 30 mil pessoas
CoronaVac (China)
A candidata da chinesa Sinovac é testada no Brasil com o apoio do Instituto Butantan (SP). Ela teve seus primeiros resultados anunciados em junho, sem efeitos adversos graves e produção de resposta imunológica em 743 voluntários iniciais.
Ela é uma vacina de vírus inativado, o que quer dizer que é feita a partir do vírus morto ou por partes dele – incapazes de se replicar. No final de agosto, o governo chinês autorizou o uso emergencial desta vacina no país para pacientes expostos ao risco, como trabalhadores da saúde e agentes de fronteira (veja o vídeo abaixo).
China aprova uso emergencial da vacina Coronavac em pacientes de alto risco
BNT162 (EUA e Alemanha)
A candidata da farmacêutica norte-americana Pfizer, desenvolvida em parceria com a empresa de biotecnologia alemã BioNTech, também usa o mRNA para codificar proteínas virais. Ela começou a ser testada na Fase 3 no final de julho.
A candidata é testada em voluntários brasileiros desde o começo de agosto e ela se mostrou promissora em sua fase inicial. Um artigo publicado no dia 20 de julho como prévia (pré-print), apontou que a substância é segura e capaz de induzir resposta imunológica.

Brasil não tem tecnologia para produzir vacina como a Pfizer, diz infectologista
Sinopharm (China)
Testada nos Emirados Árabes, a vacina da Sinopharm em parceria com o Instituto de Produtos Biológicos de Wuhan poderá estar pronta no final de 2020, segundo executivos da farmacêutica. A candidata a vacina chinesa será testada no Brasil em um acordo com o governo do estado do Paraná.
A Sinopharm também testa uma segunda candidata de vírus inativado, feita com o Instituto de Produtos Biológicos de Pequim: 5 mil voluntários nos Emirados Árabes já foram vacinados e outros 5 mil receberam a imunização na capital chinesa.
Paraná faz parceria com empresa chinesa para teste e produção de vacina contra a Covid-19
AD5-nCov (China)
A candidata chinesa da CanSino Biological, uma das quatro testadas no Brasil, está na sua terceira fase clínica. A AD5-nCov começou sua prova de segurança logo em março com um ensaio controlado com 500 participantes em que provou que induz a criação de anticorpos.
Os resultados das pesquisas devem ser divulgados entre dezembro de 2020 e janeiro de 2021, segundo os cientistas, mas antes disso, o governo chinês já concedeu sua primeira patente, isso significa que a CanSino tem a propriedade sobre a vacina e o direito de vender as doses.
Vacina da chinesa CanSino Biologics é segura e induz resposta imune, apontam testes
Ad26 SARS-Cov-2 (EUA)
A candidata norte-americana da Janssen Pharmaceutical, que recebeu autorização da Anvisa para ser testada no Brasil, também está em sua terceira e última fase de testes em humanos. Ainda não há informações sobre voluntários ou institutos responsáveis pela aplicação dos testes.
NVX-CoV2373 (EUA)
A segunda candidata norte-americana a entrar na última fase de testes é da empresa de biotecnologia Novavax. De acordo com a companhia, o imunizante tem duas doses que, na primeira fase, apresentaram “resposta robusta” de anticorpos e “foram bem toleradas” pelos 131 voluntários que participaram da pesquisa.
O método testado pela Novavax se chama “vacina recombinante”. A empresa usou engenharia genética para cultivar réplicas inofensivas da proteína que o novo coronavírus usa para entrar nas células do corpo em meio a células de insetos, em laboratório. Os cientistas extraíram, purificaram a proteína e a embalaram em nanopartículas do tamanho do vírus.
Etapas para a produção de uma vacina
Para se produzir uma vacina, leva tempo. A mais rápida desenvolvida até o momento foi a vacina contra a caxumba, que precisou de cerca de quatro anos até ser licenciada e distribuída para a população.
/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2020/r/O/2NkuaqTk6PCulf2b5RTg/2020-07-14t152707z-1552980896-rc23th9w16br-rtrmadp-3-health-coronavirus-antibodies-vaccines.jpg)
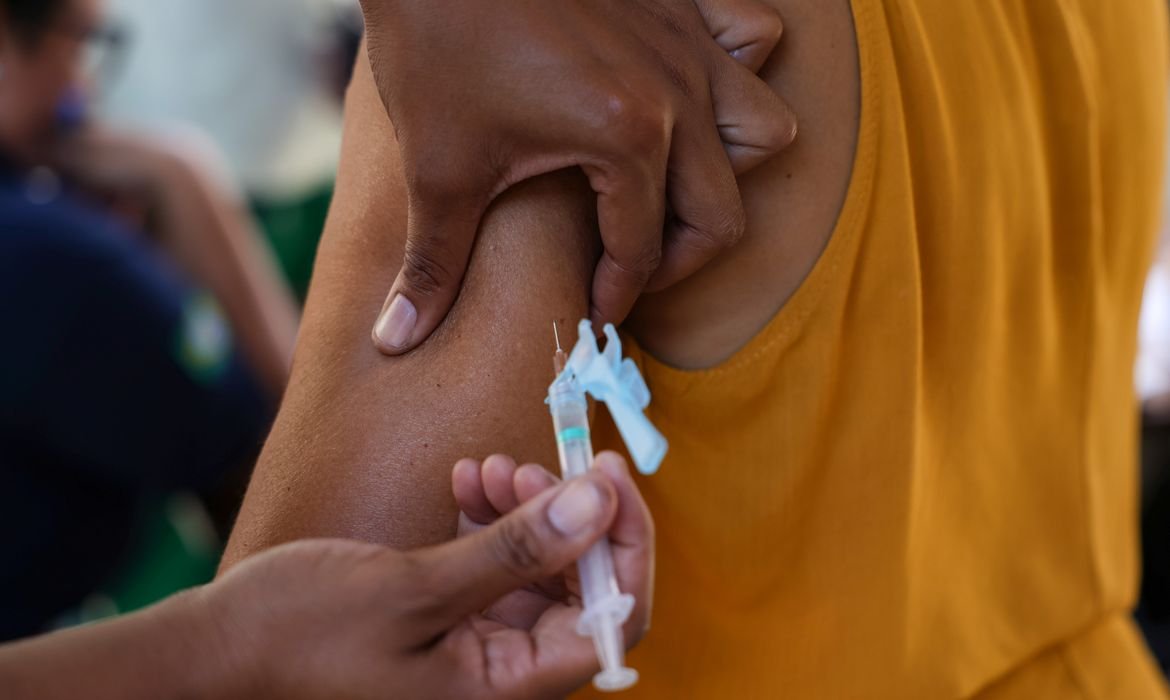
Injeção com vacina em teste para o coronavírus é aplicada na Alemanha — Foto: Kai Pfaffenbach/Reuters/Arquivo
Antes de começar os testes em voluntários, a imunização passa por diversas fases de experimentação pré-clinica (em laboratório e com cobaias). Só após ser avaliada sua segurança e eficácia é que começam os testes em humanos, a chamada fase clínica – que são três:
- Fase 1: é uma avaliação preliminar da segurança do imunizante, ela é feita com um número reduzido de voluntários adultos saudáveis que são monitorados de perto. É neste momento que se entende qual é o tipo de resposta que o imunizante produz no corpo. Ela é aplicada em dezenas de participantes do experimento.
- Fase 2: na segunda fase, o estudo clínico é ampliado e conta com centenas de voluntários. A vacina é administrada a pessoas com características (como idade e saúde física) semelhantes àquelas para as quais a nova vacina é destinada. Nessa fase é avaliada a segurança da vacina, imunogenicidade (ou a capacidade da proteção), a dosagem e como deve ser administrada.
- Fase 3: ensaio em larga escala (com milhares de indivíduos) que precisa fornecer uma avaliação definitiva da sua eficácia e segurança em maiores populações. Além disso, feita para prever eventos adversos e garantir a durabilidade da proteção. Apenas depois desta fase é que se pode fazer um registro sanitário.
Segundo a Agência Nacional de Vigilância Sanitária (Anvisa) para se fazer um ensaio clínico no Brasil, é preciso da aprovação do Comissão Nacional de Ética em Pesquisa (Conep), órgão vinculado ao Ministério da Saúde. Os voluntários são recrutados pelos centros de pesquisa.